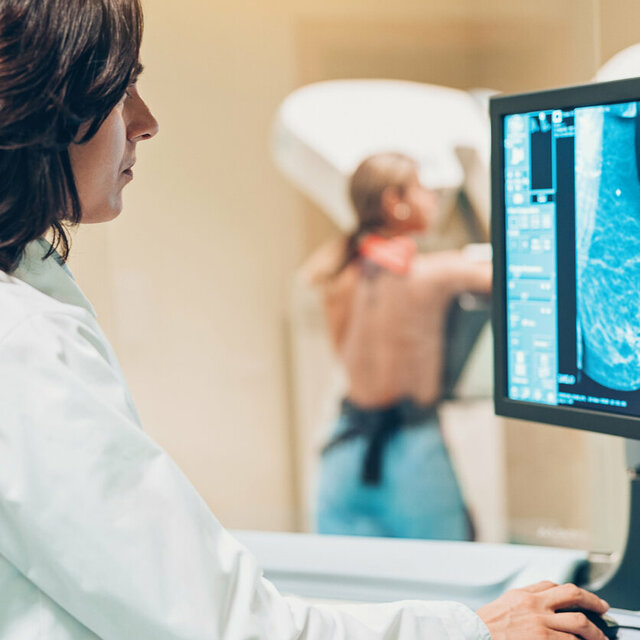
Expertise und Erfahrung aus mehr als 40 Jahren Forschung
Die GBG Forschungs GmbH gehört weltweit zu den führenden Brustkrebs-Forschungsinstituten. In diesem Institut werden die klinischen Studien der German Breast Group operativ durchgeführt.
Unser Grundprinzip lautet: Wir sind unabhängig, akademisch orientiert und neutral.
Schwerpunkt unserer Forschung sind Studien mit akademischer Fragestellung, deren Konzepte aus der praktischen Tätigkeit wissenschaftlich aktiver Ärztinnen und Ärzte hervorgehen. Im Gegensatz zu Studien, die von Arzneimittelherstellern initiiert werden, steht eine Zulassung eines Wirkstoffes bei unseren Studienkonzepten weniger im Vordergrund. Wir sind eine Academic Research Organisation (ARO).


Entwicklung moderner Therapieverfahren
Mehr als 1.000 Ärztinnen und Ärzte in über 800 Zentren sind Mitglied der Studiengruppe. Jedes Jahr nehmen mehr als 3.500 neue Patientinnen an Studien der GBG teil. In der Vergangenheit wurden klinische Daten von über 67.000 Frauen mit Brustkrebs gesammelt.
Renommierte Brustkrebs-Experten der GBG organisieren sich in Subboards, um die besten Studienkonzepte zu entwickeln. Hier entstehen neue Studienideen, die gemeinsam mit Studienzentren in Deutschland und in der ganzen Welt umgesetzt werden.
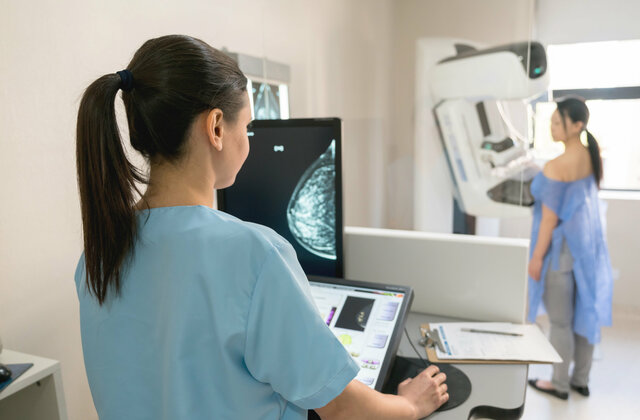
Ich habe mich für die GBG als Arbeitgeber entschieden, weil sie eine schnell wachsende und internationale Firma ist, - damit kann auch ich selbst noch wachsen!
Entwickle mit uns modernste Therapieansätze für Brustkrebs-Patientinnen

Fragen, die sich vor der Teilnahme an einer klinischen Studie stellen
1. Was ist eine Studie?
Klinische Studien werden durch international anerkannte Fachärzte an spezialisierten Brustkrebszentren und Kliniken durchgeführt. Dabei werden neueste Behandlungsarten und Wirkstoffe geprüft, um die Therapie von Brustkrebspatientinnen weiter zu verbessern. Ziel ist es, zunehmend individuellere und wirksamere Therapien zu finden.
2. Was bringt es mir, an einer Studie teilzunehmen?
Patientinnen mit Brustkrebs, die an einer Studie teilnehmen, haben die Chance, frühzeitig innovative Behandlungsmethoden zu bekommen, die im klinischen Alltag noch nicht verfügbar sind.
Es ist ein Qualitätsindikator, wenn ein Brustzentrum an klinischen Studien mitwirkt. Indem Sie aktiv teilnehmen, können Sie am Therapiefortschritt teilhaben.
3. Wie kann ich teilnehmen?
Jeder Brustkrebs hat seine eigenen Merkmale, für die maßgeschneiderte und zielgerichtete Therapien entwickelt werden. Bei der GBG sind eine Reihe von Studien aktiv, die möglicherweise für Sie in Frage kommen. Mehr dazu finden sie auf der Patientinnen-Seite.